明治大学大学院農学研究科 環境バイオテクノロジー研究室の研究グループ
明治大学大学院農学研究科環境バイオテクノロジー研究室の井関夏奈子(博士前期課程1年)、小山内崇准教授らの研究グループは、モデルラン藻であるシネコシスティスを用い、明好気条件下での高密度な培養により、効率的なフマル酸生産技術を開発しました。
<研究成果のポイント>
・シネコシスティスは、二酸化炭素を原料として、バイオプラスチックの原料などに利用されるフマル酸を直接生産できる。
・従来の簡便な明好気条件下での生産法では、フマル酸の生産量はわずか150 mg/L未満にとどまり、生産性の向上が課題であった。
・本研究では、培地濃度の増加による高密度培養と、フマル酸生産方向への代謝フラックスの増強を組み合わせることで、フマル酸を高純度で生産し、シネコシスティスにおける最高記録となる2 g/L以上を達成した。
要旨
光合成細菌の一種であるラン藻は、大気中の二酸化炭素を取り込みながら増殖し、さまざまな有用物質を生産できることから、持続可能なバイオものづくりの担い手として近年注目されています。
本研究グループはこれまでに、ラン藻の一種であるシネコシスティス注1)を用いて、発酵による有用化合物の生産を行ってきました。特に、バイオプラスチックなどの原料となるフマル酸などのカルボン酸が、発酵によって細胞外に放出されることを明らかにしてきました。しかし、従来の発酵による生産方法では、複数段階の培養工程を必要とするため、実用化に向けては工程の簡略化やコスト面での改善が課題となっています。そこで、複雑な工程を経ず、光と酸素が存在する明好気条件下でフマル酸を生産する手法が検討されています。
海外の研究グループは、フマル酸を別の物質へ変換する酵素であるフマラーゼ(FumC)を欠損させたシネコシスティスにおいて、明好気条件でフマル酸を細胞外に排出することを報告しました注2)。しかし、その最大生産量はわずか150 mg/L未満にとどまっており、生産量の向上が求められています。
そこで本研究グループは、生産量向上のために2つのアプローチを行いました。第一に、シネコシスティス自体のバイオマス(細胞量)を増加させることを目的として、高密度培養を検討しました。第二に、フマル酸へいたる代謝の流れ(代謝フラックス)を強化するため、FumCの欠損とともに、フマル酸に至る上流の代謝経路の酵素(ホスホエノールピルビン酸カルボキシラーゼ、PEPC)を過剰発現させる遺伝子改変を行いました。その結果、培地中の栄養成分濃度を10倍に高めた条件において、遺伝子改変株は最大2046 mg/Lのフマル酸を生産しました。また、シネコシスティスが生産した全有機酸のうち、フマル酸は87%を占めており、高い純度でフマル酸が生産されていることが示されました。
以上の結果から、本研究では、1.高密度培養によるバイオマスの制限の克服と、2.代謝フラックスをフマル酸方向へ集中させる代謝設計を行うという2つの戦略を組み合わせることで、シネコシスティスによるフマル酸の高純度かつ最高記録(2 g/L以上)の生産を達成しました。
本研究は、明治大学大学院農学研究科 環境バイオテクノロジー研究室の井関夏奈子(博士前期課程1年)、小山内崇准教授らの研究グループによって行われました。また、本研究はJST革新的GX技術創出事業(代表:大熊盛也)、旭硝子財団(代表:小山内崇)の援助により行われました。本研究成果は、2026年3月12日に国際誌「Microbial Cell Factories」のオンライン版に掲載されました。
※研究グループ
明治大学大学院農学研究科環境バイオテクノロジー研究室
准教授 小山内 崇(おさない たかし)
博士前期課程1年 井関 夏奈子(いせき かなこ)
専門研究員 飯嶋 寛子(いいじま ひろこ)
研究技術員 大根田 聡子(おおねだ さとこ)
1.背景
近年、地球温暖化の進行や化石資源の枯渇といった課題を背景に、二酸化炭素の排出を抑えつつ資源を循環させる、カーボンニュートラルな社会の実現が強く求められています。その実現に向けた技術の一つとして、光合成細菌であるラン藻を利用したバイオものづくりが注目されています。
ラン藻は、大気中の二酸化炭素を光合成によって固定しながら増殖し、有用な化合物を生産する能力を有しています。この特性を活用すれば、二酸化炭素を原料として物質を生産できるため、温室効果ガスの削減と化石資源依存の低減の両立が可能になると期待されています。
本研究グループはこれまでに、ラン藻の一種であるシネコシスティスを用い、発酵条件下でフマル酸、リンゴ酸、コハク酸などの有機酸を合成できることを見出しました。これらの有機酸はカルボン酸と呼ばれ、バイオプラスチックをはじめとする化学工業原料として広く利用されています。しかし、現在工業的に利用されているカルボン酸の多くは化石資源を原料として生産されています。
本研究グループがこれまでに報告したカルボン酸生産法では、まず明所で光合成により細胞を増殖させた後、窒素を制限した培地で培養し、固定した二酸化炭素をグリコーゲンとして細胞内に蓄積させます。その後、暗所かつ無酸素条件である「発酵条件」に移行させることで、蓄積したグリコーゲンをカルボン酸へと変換させます(図1)。しかし、この方法では培養工程が複数段階に分かれており、操作の煩雑さや設備面での制約が課題となっています。
そこで近年では、このような発酵工程を経ず、光と酸素が存在する明好気条件下でカルボン酸を直接生産する手法が世界的に検討されています。
海外の研究グループは、カルボン酸の一種であるフマル酸の生産において、フマル酸からリンゴ酸へと変換する酵素であるフマラーゼ(FumC)を欠損させたシネコシスティスが、明好気条件下でフマル酸を細胞外へ排出することを報告しました。しかし、その最大生産量は139 mg/Lにとどまっており、さらなる生産性の向上が求められています。
フマル酸の生産量が低い要因としては、シネコシスティス自体のバイオマス(細胞量)が少ないことに加え、フマル酸へ至る代謝フラックス(代謝の流れ)が十分でないことが挙げられます。そこで本研究では、これら2つの課題を解決することで、フマル酸の生産性向上を目指しました。
2.研究手法と成果
本研究グループは、まずシネコシスティスの野生株とFumC欠損株を明好気条件下で培養しました。その結果、FumC欠損株は野生株と比較して光合成活性が向上しており、さらにFumC欠損株においてのみフマル酸が細胞外へ排出されることを確認しました(図2)。
次に、シネコシスティスのバイオマスの制限を克服するため、FumC欠損株の高密度での培養を検討しました。通常用いられるBG-11培地に対し、栄養成分濃度を10倍に高めた培地(×10 BG-11)を用いて培養した結果、培養16日にフマル酸を最大1399 mg/L排出しました。なお、フマル酸は、検出された有機酸全体の85%を占めていました(図3)。
さらに、フマル酸生産をより促進するため、代謝フラックスの増強にも取り組みました。ラン藻では、フマル酸を生成するクエン酸回路への炭素フラックスが他の生物と比較して低いことが知られています。そこで、光合成とは別経路で二酸化炭素を固定し、クエン酸回路の基質を供給する酵素であるホスホエノールピルビン酸カルボキシラーゼ(PEPC)に着目しました。FumC欠損株にPEPCを過剰発現させた遺伝子改変株(FumC欠損/PEPC過剰発現株)を作製し、フマル酸の生産性を評価しました。
その結果、FumC欠損/PEPC過剰発現株は、培養16日にフマル酸を最大2046 mg/L排出しました。また、フマル酸は有機酸全体の87%を占めていました。これは、代謝改変により炭素の流れがフマル酸合成方向へ効果的に再配分されたことを示唆しています(図4)。
3.今後の期待
本研究では、1.高密度培養による細胞量の制限の克服と2.炭素フラックス制御による代謝強化という2つのアプローチを組み合わせることで、シネコシスティスによるフマル酸の高純度かつ最高記録(2 g/L以上)の生産を達成しました。
一方で、シネコシスティスにおいてフマル酸はクエン酸回路に加え、アミノ酸合成経路など複数の代謝経路を通じても生産されます。FumC欠損株において、フマル酸が主にどの代謝経路を経て生産されているのかは、現時点では十分に解明されていません。そのため、フマル酸の主要な生産経路を明らかにすることが、さらなる生産性向上に向けた重要な課題です。
今後は、フマル酸の主要な代謝経路を解明するとともに、本研究で確立した高密度培養および代謝制御の戦略を組み合わせることで、さらなるフマル酸生産量の向上が期待されます。
4.論文情報
<タイトル>
Enhanced fumarate production using high-density cultivation of Synechocystis sp. PCC 6803(Synechocystis sp. PCC 6803の高密度培養によるフマル酸生産の増強)
<著者名>
Kanako Iseki, Hiroko Iijima, Satoko Ohneda, Takashi Osanai
<雑誌>
Microbial Cell Factories
<DOI>
10.1186/s12934-026-02956-5
5.補足説明
注1)シネコシスティス
世界で最も広く研究されている単細胞性ラン藻の一種。淡水性で、窒素固定は行わない。1996年にラン藻として初めて全ゲノム配列が決定された。ほかの微細藻類と比較して増殖が速く、遺伝子改変が容易で、凍結保存が可能であるなど、実験生物として多くの利点を有する。学名はSynechocystis sp.。
注2)参考文献
Du W, Jongbloets JA, Guillaume M, van de Putte B, Battaglino B, Hellingwerf KJ, Branco Dos Santos F (2019) Exploiting day- and night-time metabolism of Synechocystis sp. PCC 6803 for fitness-coupled fumarate production around the clock. ACS Synth Biol 8:2478-2486.
https://pubs.acs.org/doi/10.1021/acssynbio.9b00289
[参考図]
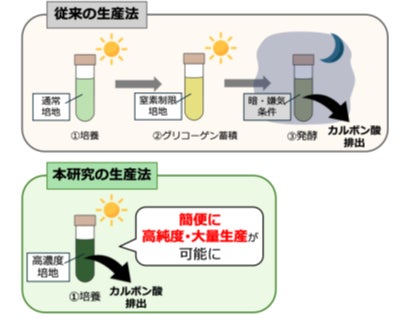
図1. シネコシスティスによるカルボン酸の生産法
過去に報告された生産法では、1.明所で培養、2.細胞を窒素を制限した培地に移してグリコーゲンを蓄積、3.暗所・無酸素条件(発酵条件)という3工程を経てカルボン酸を生産します(上図)。一方、本研究での生産法は、1.明所で培養のみの1工程で、カルボン酸を高純度で大量生産が可能です(下図)。
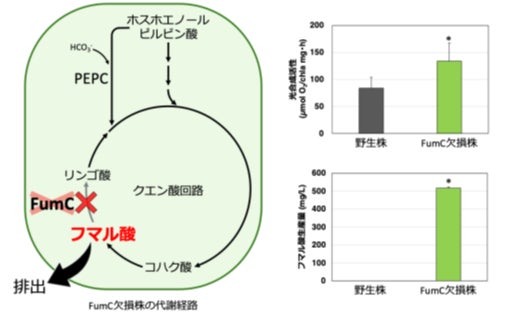
図2. FumC欠損株の代謝特性
フマル酸からリンゴ酸に変換する酵素FumCを欠損させることで、フマル酸が細胞外へ排出されることが知られています。FumC欠損株は野生株に比べて光合成活性が上昇し、野生株ではフマル酸の排出は確認されなかったのに対し、FumC欠損株ではフマル酸の排出が確認されました。アスタリスクは、野生株とFumC欠損株の間に統計的有意差があることを示しています(*p<0.05)。
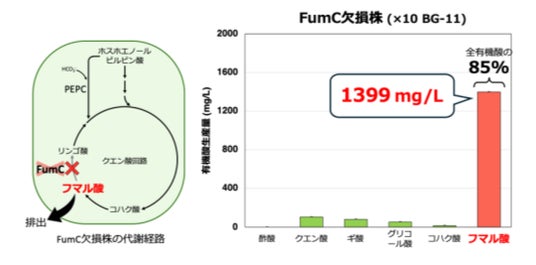
図3. ×10 BG-11におけるFumC欠損株の有機酸生産量
FumC欠損株は、酢酸、クエン酸、ギ酸、グリコール酸、コハク酸、フマル酸の6種類の有機酸を生産しました。そのうちフマル酸は1399 mg/L生産され、全有機酸の85%を占めていました。
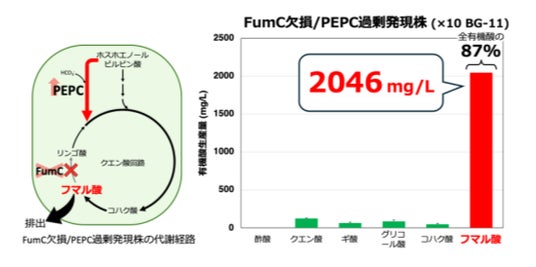
図4. ×10 BG-11におけるFumC欠損/PEPC過剰発現株の有機酸生産量
FumC欠損株にPEPCを過剰発現させることで、フマル酸合成への代謝フラックスの増強を試みました。FumC欠損/PEPC過剰発現株は、酢酸、クエン酸、ギ酸、グリコール酸、コハク酸、フマル酸の6種類の有機酸を生産しました。そのうちフマル酸は2046 mg/L生産され、全有機酸の87%を占めていました。
 公式フェイスブックページ
公式フェイスブックページ