令和8年5月15日
国立大学法人徳島大学
https://www.tokushima-u.ac.jp/
■ポイント
・自己免疫疾患を加速する“細胞間クロストーク”を解明
・従来脇役と考えられていた線維芽細胞※1が病態の主導因子であることを発見
・新規治療標的(CD153-CD30経路)を提示し創薬への道を開拓
■概要
自己免疫疾患は、免疫系が自分自身の組織を攻撃してしまうことで発症し、慢性的な炎症を引き起こす難治性疾患です。しかし、炎症が持続的に増幅され病態が進展する機序についての詳細は解明されていません。徳島大学大学院医歯薬学研究部(医学域)・生体防御医学分野 教授/フォトニクス健康フロンティア研究院 最高研究責任者(CRO)の安友康二氏、徳島大学病院歯科口腔外科 助教(研究当時/現 Monash University研究員)の大塚邦紘氏らの研究グループは、自己免疫疾患であるシェーグレン病において、CD153※2を発現するCD4陽性T細胞※3と組織常在線維芽細胞との相互作用が炎症を増幅する新たなメカニズムを明らかにしました。
本研究では、単一細胞RNA解析などを用いて病変組織内の細胞動態を詳細に解析した結果、CD153陽性CD4T細胞が線維芽細胞上のCD30と結合し、線維芽細胞の増殖及びCXCL13やCCL19といったケモカインの産生を誘導することを見出しました。これにより免疫細胞のさらなる集積が促進され、炎症が持続的に増幅されることが明らかとなりました。さらに、この相互作用を阻害することで炎症細胞の浸潤や組織障害が有意に抑制されることを示し、本経路が病態の進展に重要であることを実証しました。
本研究は、免疫細胞と非免疫細胞との相互作用が自己免疫疾患の進行に果たす役割を明らかにしたものであり、CD153-CD30経路を標的とした新たな治療戦略の開発につながることが期待されます。本成果は、2026(令和 8)年 5 月 12 日付けで『Nature Communications』のオンライン版に掲載されました。
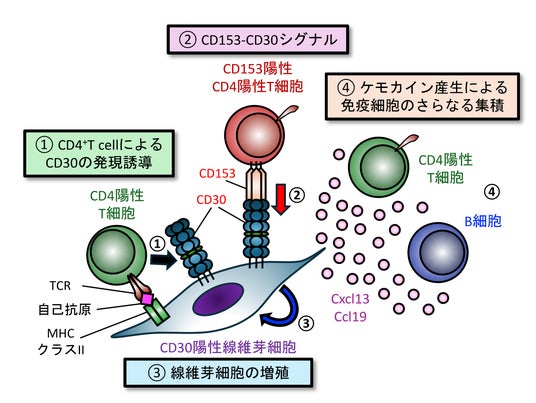
研究の概略図唾液腺に浸潤したCD4陽性T細胞が線維芽細胞のCD30発現を誘導する。その後、CD153を発現するCD4陽性T細胞とCD30が相互作用することにより、線維芽細胞の細胞増殖と各種ケモカインの産生が促される。その際に、CD153陽性T細胞は自己抗原を認識して増殖が促されていると推測される。以上の相互作用と細胞応答の結果、組織を破壊するT細胞やB細胞などが唾液腺臓器内に集積することにより、病態の進展が促される。
■研究の背景と経緯
自己免疫疾患は、本来外敵から身体を守るべき免疫系が、自分自身の組織を攻撃してしまうことで発症し、慢性的な炎症と組織障害を引き起こす難治性疾患です。中でもシェーグレン病は、涙腺や唾液腺などの外分泌腺にリンパ球が浸潤し、ドライアイやドライマウスといった症状を呈する代表的な自己免疫疾患です。
これまで、自己免疫疾患の発症や進展にはCD4陽性T細胞を中心とした免疫細胞の異常が重要であると考えられてきました。しかし近年、組織を構成する線維芽細胞などの非免疫細胞も、単なる支持構造ではなく、免疫応答を積極的に制御する可能性が指摘され始めています。特に、炎症局所に形成される三次リンパ組織においては、線維芽細胞が免疫細胞の集積や局所免疫応答の形成に関与することが示唆されてきましたが、その分子機構や細胞間相互作用の詳細は不明な点が多く残されていました。
このような背景のもと、本研究では、自己免疫疾患の進行を規定する新たな細胞間相互作用の解明を目指し、免疫細胞と組織細胞のクロストークに着目しました。特に、シングルセル解析技術を用いて病変組織内の細胞動態を網羅的に解析し、病態形成に関与する新たな細胞集団及び相互作用の同定を試みました。
■研究の内容と成果
本研究では、シェーグレン病モデルマウス及び患者検体を用い、単一細胞RNA解析や組織学的解析を組み合わせることで、病変局所における細胞間相互作用を詳細に解析しました。その結果、CD153を発現する特異的なCD4陽性T細胞集団が病変初期から増加し、炎症の進展に深く関与していることを明らかにしました。さらに、このCD153陽性CD4T細胞が、組織内の線維芽細胞上に発現する受容体CD30と直接相互作用することを見出しました。この相互作用により、線維芽細胞は活性化され、増殖するとともにCXCL13やCCL19といったケモカインを産生するようになります。これらのケモカインはT細胞やB細胞の集積を誘導し、炎症局所における免疫細胞のさらなる集積と三次リンパ組織の形成を促進します。以上のメカニズムはヒト組織切片でも検証され、同様の病態が観察されました。
重要な点として、本研究では、このCD153-CD30経路を阻害することにより、線維芽細胞の増殖やケモカイン産生が抑制され、結果として炎症細胞の浸潤及び組織障害が有意に軽減されることを示しました。すなわち、本研究は、免疫細胞のみならず組織細胞が積極的に炎症を増幅するという新たな病態モデルを提示するとともに、特定の細胞間相互作用が自己免疫疾患の進行を駆動することを実証したものです。
■今後の展開
本研究により同定されたCD153陽性CD4T細胞とCD30陽性線維芽細胞の相互作用は、自己免疫疾患における炎症増幅の中核的な機構である可能性が示されました。この知見は、従来の「免疫細胞中心」の病態理解を拡張し、組織細胞を含めた細胞間ネットワークとして自己免疫疾患を捉える新たな視点を提供するものです。今後は、このCD153-CD30経路を標的とした分子標的治療の開発が期待されます。すでに本研究では、この経路の阻害によって病態が改善することを実験的に示しており、抗体医薬などへの応用可能性が考えられます。また、本研究で明らかとなった線維芽細胞の免疫制御機能は、シェーグレン病に限らず、関節リウマチや全身性エリテマトーデスなど他の自己免疫疾患にも共通する可能性があり、広範な疾患への波及効果が期待されます。さらに、シングルセル解析や空間解析技術を活用することで、病変組織内の細胞間相互作用をより精緻に理解し、個々の患者に応じた精密医療の実現にもつながると考えられます。本研究は、自己免疫疾患の病態理解と治療戦略の両面において、新たな展開を切り拓く成果と位置付けられます。
■研究プロジェクトについて
本研究は、日本学術振興会 J-PEAKS (JPJS00420240022)、科学研究費助成事業(20K18479、23K15976、23H00438)AMED生命科学・創薬研究支援基盤事業、武田科学振興財団の支援を受けて実施されました。
■用語解説
※1)線維芽細胞:皮膚や臓器などの組織に広く存在し、コラーゲンなどの細胞外マトリックスを産生して組織構造を維持・修復する細胞です。従来は構造維持の役割が中心と考えられていましたが、近年では炎症や免疫応答の制御にも関与することが分かってきました。
※2)CD153:T細胞などの免疫細胞の表面に発現するタンパク質で、CD30という受容体と結合することで細胞間の情報伝達を担う分子です。特に慢性炎症や加齢に伴う免疫応答との関連が知られています。
※3) CD4陽性T細胞(CD4T細胞):免疫応答の司令塔として働くリンパ球の一種で、他の免疫細胞の活性化や調節を担います。感染防御に重要な役割を果たす一方で、自己免疫疾患では過剰に活性化し、自身の組織を攻撃する原因となります。
■論文情報
掲載誌: Nature Communications
論文名:
A CD4+ T cell-fibroblast crosstalk exacerbates autoimmunity in primary Sjogren disease
著者名:
Kunihiro Otsuka, Hiroyuki Kondo, Shin-Ichi Tsukumo, Daisuke Kurotaki, Kei-ichiro Yasunaga,
Aya Ushio,Ruka Nagao, Keiko Aota, Yoshiaki Kitamura, Takaaki Tsunematsu, Hideo Yagita,
Naozumi Ishimaru, Junko Morimoto, Koji Yasutomo* (* 責任著者)
DOI番号: 10.1038/s41467-026-72975-8
責任著者:
徳島大学大学院医歯薬学研究部(医学域)・生体防御医学分野 教授
徳島大学フォトニクス健康フロンティア研究院 最高研究責任者(CRO)
安友 康二
■関連リンク
・徳島大学×J-PEAKS
https://www.iphf.tokushima-u.ac.jp/
 公式フェイスブックページ
公式フェイスブックページ